定期修繕・バリデーションサポート
定期修繕サポート
各国当局他(厚労省など)の査察において、メンテナンスの運用に関する指摘や要求は毎年増大しております。
当社はグループ医薬品会社の操業・保全業務から得た知見をベースにメンテナンス項目や周期の妥当性を検討しながら文書化し、PDCAによる保全体系を構築いたします。
技術説明
-
現状調査により、既存設備の完成図書(フローシート・機器リスト・バルブリスト・計器リスト・バリデーション文書他)を確認し、設備・機器の区分や点検項目・部品交換項目を規定
-
バイオ医薬品製造工場のおける豊富な実績を基に、必要に応じてリスクアセスメントを実施しながら、各設備の点検周期及び部品交換周期を決定。
-
抜け漏れ無い点検を実施し、定型フォーマットの報告書サマリーを作成。(保守点検のトレースの容易化)
-
報告書サマリーから、各設備の部品交換周期を評価し、かつ日常のトラブル状況を今後の定修計画に反映。
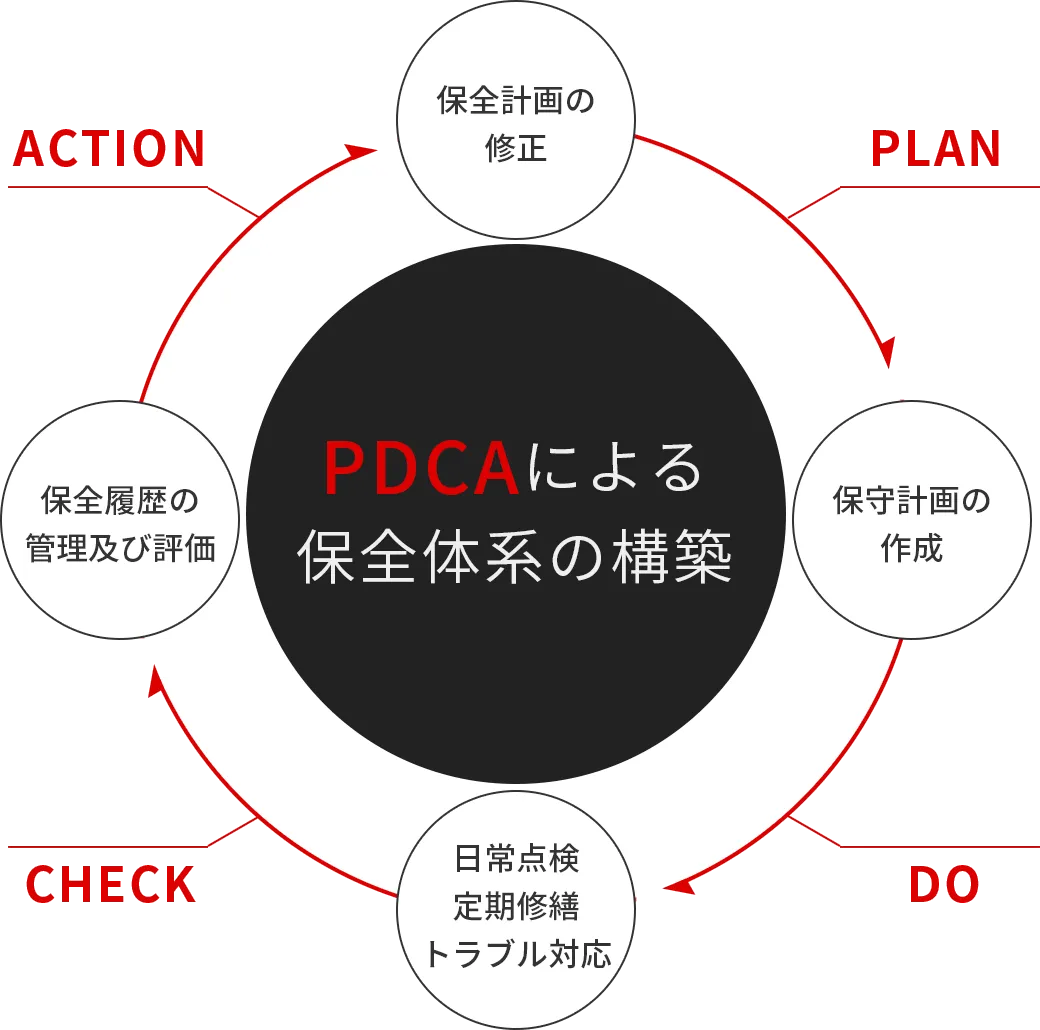
特長
予防保守を目的とした計画策定から実行、文書の整備により、製品品質の担保及び安定操業に貢献いたします。
-
機器分類表

-
TBMカレンダー
-
保守点検成績表
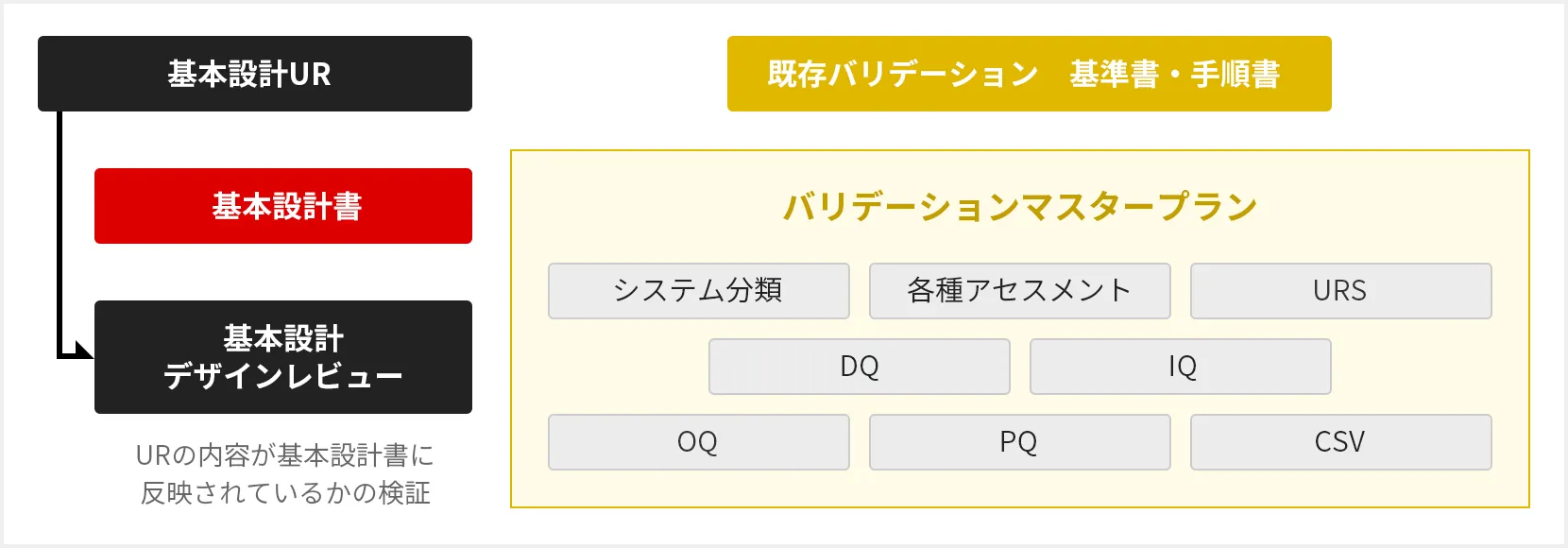
バリデーションサポート
コミッショニング&クオリフィケーション(C&Q)の思想により、お客様のバリデーション負荷低減や
リスクベースアプローチを取り入れた文書体系を構築し、最新のGMPに対応します。
技術説明
-
システムインパクトアセスメントを実施し、製品品質に直接影響を与えるシステムをGMP対象設備とし、その他システムをnon-GMP設備に区分。
-
non-GMP設備はGEP範疇とし、バリデーション 対象外とすることでお客様の負荷を低減。
-
リスクベースアプローチとして、リスクアセスメントを 実施し、URSに反映、さらにDQ/IQ/OQでリスクアセスメント結果を検証。
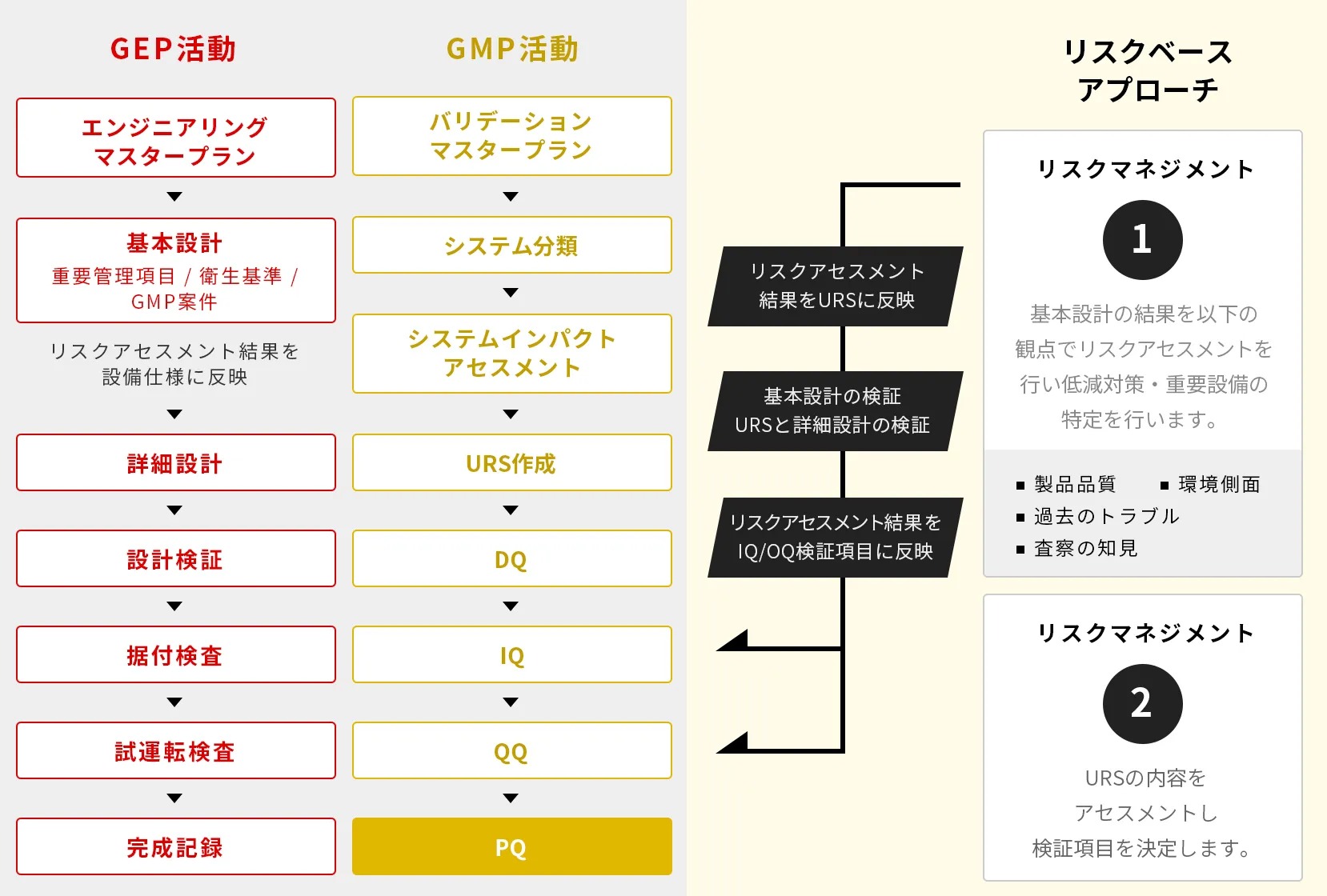
特長
Good Manufacturing Practice(GMP)活動における文書については、Good Engineering Practice (GEP)活動とも密接に関わるため、バリデーションマスタープラン(VMP)作成から、稼動時適格性確認(PQ)までの各文書の作成助成を行います。